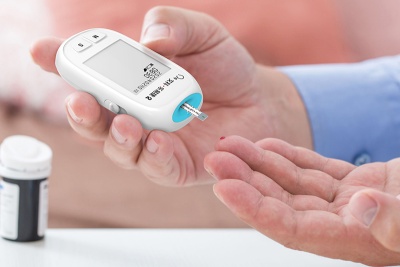
包材类DMF范围有哪些?
包材类DMF(Drug Master File)是提交给美国食品药品监督管理局(FDA)的一种文件,专门用于提供关于药品包装材料和容器的详细信息。
一、基本信息部分
1.企业信息
包括包材生产企业的名称、地址、联系方式、企业性质(如股份制、独资等)、生产规模(年产量、生产车间数量等)。这些信息有助于监管机构和药品企业了解包材的来源,评估企业的生产能力和稳定性。
2.包材产品信息
详细介绍包材的名称、型号、规格,例如对于塑料瓶,要说明其容量大小(如100ml、250ml等)、形状(圆形、方形等)、颜色(透明、棕色等)。同时,还需提供包材的用途,是用于固体药物包装(如片剂、胶囊)还是液体药物包装(如糖浆、注射液),或者是用于特殊剂型(如气雾剂、贴剂)的包装。
3.质量体系信息
阐述企业的质量管理体系,如是否通过ISO质量管理体系认证(如ISO 9001),以及在包材生产过程中所遵循的质量标准和规范。这包括原材料采购的质量控制、生产过程中的质量检验流程和成品的质量检验标准等内容,以确保包材质量的一致性和可靠性。
二、 原材料部分
1.化学成分
对于玻璃包材,要说明玻璃的主要成分,如二氧化硅(SiO₂)的含量、碱金属氧化物(如氧化钠Na₂O、氧化钾K₂O)的含量等。对于塑料包材,需明确聚合物的种类(如聚乙烯PE、聚丙烯PP、聚氯乙烯PVC等)和添加剂(如增塑剂、抗氧剂、着色剂等)的化学成分。金属包材则要提供合金成分(如铝 镁合金中镁的含量等)。这些化学成分信息对于评估包材的化学稳定性、与药品的相容性至关重要。
2.原材料来源
记录每种原材料的供应商名称、地址、联系方式。同时,要说明原材料的质量标准,是否有供应商提供的质量检验报告,以及企业自身对原材料进行的检验项目和频率。例如,对于塑料包材的聚合物原料,要检查其分子量分布、杂质含量等指标。
三、 物理性能部分
1.机械性能
测试并记录包材的机械强度,如抗张强度、抗压强度和抗冲击强度。以塑料瓶为例,抗张强度测试可以确定瓶子在受到拉伸力时的承受能力,抗压强度则是衡量瓶子在堆叠或受到外部压力时是否会变形或破裂的指标,抗冲击强度对于在运输过程中可能受到碰撞的包材非常重要。
2. 阻隔性能
评估包材对气体(如氧气、二氧化碳)、水汽和光线的阻隔能力。对于一些对氧气敏感的药品(如某些抗生素、维生素等),包装材料需要有良好的氧气阻隔性,以防止药品氧化变质。对于含有挥发性成分的药品或需要防潮的药品,水汽阻隔性能就显得尤为重要。而对于一些光敏感的药品(如某些眼药水、硝酸甘油片等),包装材料的遮光性是关键,要说明包材的透光率等指标。
3.尺寸和形状稳定性
提供包材的尺寸公差范围,如瓶子的直径、高度的允许误差。同时,要说明在不同环境条件(如温度、湿度变化)下,包材的形状是否会发生变化,例如塑料包装在高温下是否会变形,影响药品的包装效果和质量。
四、生产工艺部分
1.生产流程
详细描述包材从原材料到成品的整个生产过程,包括各个生产步骤的顺序、工艺参数(如温度、压力、时间等)。以玻璃瓶生产为例,要说明玻璃原料的熔化温度、成型时的吹制压力和时间等参数。对于塑料包材,要描述注塑或吹塑过程中的模具温度、注射速度等。
2.质量控制环节
在生产过程中,企业应设置多个质量控制节点。例如,在原材料投入生产前的检验、生产过程中的中间产品检验(如塑料瓶吹塑过程中的瓶坯检验)和成品检验。要说明每个检验节点所采用的检验方法(如物理性能测试方法、化学分析方法)和检验标准(如合格的指标范围)。

五、稳定性部分
1.化学稳定性
研究包材在不同化学环境下的稳定性,例如,当包材接触到药品中的活性成分、辅料(如酸性或碱性辅料)时是否会发生化学反应。通过模拟不同的化学环境进行实验,观察包材的化学性质变化,如是否会释放出有害物质、自身是否会被腐蚀等。
2. 物理稳定性
考察包材在长期储存和不同环境条件下的物理性能变化。例如,经过长时间的储存,塑料包材是否会出现老化现象(如变脆、变色),玻璃包材是否会出现脱片现象等。同时,还要考虑在运输过程中的物理稳定性,如在颠簸、震动等条件下包材的完整性。
六、安全性部分
1. 生物安全性
评估包材对人体是否存在潜在的生物危害。例如,包材中的某些化学成分是否会迁移到药品中,这些迁移物是否会对人体产生毒性、刺激性或过敏反应。通过进行生物相容性测试(如细胞毒性试验、皮肤刺激性试验等)来验证包材的生物安全性。
2.环境安全性
考虑包材在生产、使用和废弃后的环境影响。例如,塑料包材是否可回收利用,其在自然环境中的降解性如何;玻璃包材在废弃后是否会产生有害物质等。这部分内容对于企业的可持续发展和环境保护也具有重要意义。