FDA认证医疗器械标签要求
FDA认证对于出现在医疗设备上的标签声明非常具体。医疗设备标签上允许的信息由设备类别法规确定,包括:FDA认证 1级,FDA认证 510(k)或FDA认证上市前批准(PMA)。根据《食品药物和化妆品法》(FDCA)的定义,医疗设备的“标签”一词不仅超出了设备上的印刷标签,还将涵盖所有设备随附的手册,手册,营销材料和网站。
超过许可,FDA认证批准或适用的FDA认证声明的索赔,将导致医疗设备跃入未经批准的医疗设备类别,因此需要FDA认证强制执行。
标签问题通常是导致FDA认证批准和出口滞留延迟的主要原因,商通检测设备标签专家团队将首先通过对您的标签与相关的美国联邦法规数据库和FDA认证标签准则进行交叉检查来分析您的标签。接下来,我们将为您提供有关医疗设备的符合FDA认证标准的全面标签审查。
查将以全包报告格式提供,其中包括建议的图形设计和准备用于产品的权利要求修改。单击最前面的启动按钮以请求免费的初始标签评估和符合FDA认证的专家级设备标签审查。
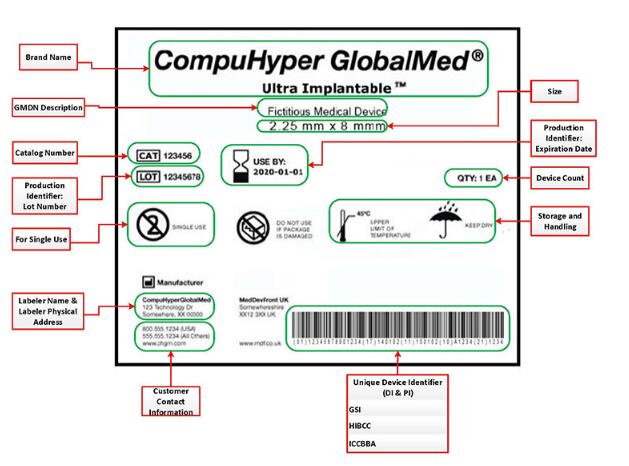
FDA认证的医疗器械标签规则是什么?
FDA认证的标签系统基于“唯一设备标识”系统,其中每个设备都会收到UDI标签。标签使用所有类型和产品标识符的设备通用的前缀。设备标识符通过访问全局唯一设备标识数据库来帮助用户跟踪项目。重复使用的医疗工具必须在设备本身上具有此标签,并且所有物品的包装上都必须具有UDI标签。这些标签反映了新的泛欧洲统一的描述性符号标准。
FDA认证批准的UDI标签将UDI代码的纯文本版本与条形码等机器可读版本结合在一起。识别码本身是与FDA认证认可的发行机构合作开发的。这些标签要求首先推广到可植入,救生和维持生命的医疗设备,然后逐步扩展到整个行业。到2020年9月24日,每种类型的设备都将需要UDI标签,包括设备本身上未处理的可重复使用物品的标签。
FDA认证标签上包含的信息超出了UDI代码,包括品牌名称,描述,尺寸,目录号,有效期,使用说明等。标签上还会显示标签商的公司名称和实际地址,以及联系信息和适用的警告。
商通检测提供医疗器械FDA认证服务,可为您检查标签是否符合FDA要求,帮您顺利进入美国市场!