水循环热/冷治疗设备FDA认证
美国食品药品监督管理局(FDA认证)已发布安全通讯,专门介绍水循环热/冷疗法设备的冷疗法模式的使用。该文档旨在提醒上述设备的用户有关遵循设备随附的使用说明以确保安全性和有效性的重要性。
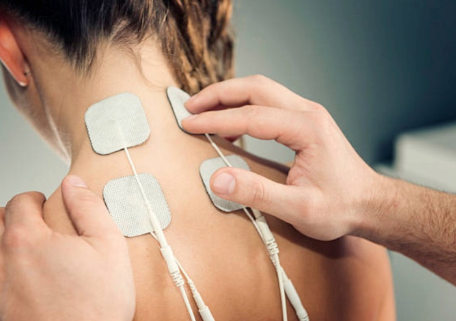
概述FDA认证安全通讯范围内的医疗设备非常重要。特别地,该文件专用于医疗设备,该医疗设备被用于产生通过管道系统的热水或冷水的流动,以向身体的特定部位提供冷热疗法。由于结构的特殊性,某些设备只能用于提供冷处理,而某些设备可以同时提供两种类型。一些设备还具有其他功能,例如在热疗或冷疗期间或单独使用时可进行压缩。根据设计和构造,水循环热/冷治疗设备还可具有可编程的时间和温度设置或自动停用功能。一般来说,这种类型的医疗设备旨在用于为患者提供暂时的疼痛缓解。这些设备可在家中或医疗机构中使用。
FDA认证安全通讯的依据:
机构指出,自2015年起连续四年,已收到15份不良事件报告,描述了以冷疗法模式运行的水循环热/冷疗法设备造成的伤害。根据FDA认证可获得的信息,在某些情况下,患者需要进行额外的医学干预以治疗这些副作用的后果。因此,该机构指出,该设备可以工作的所有模式都与某些固有风险相关联,主要表现为以压缩模式使用该设备时出现的组织伤害和/或疼痛。
FDA对患者的建议 :
为了减轻与使用热/冷处理医疗设备相关的风险,FDA认证提供了患者应遵循的某些建议。
这些建议包括:
1.在使用设备之前:请考虑要点,包括要应用的特定治疗类型,治疗的频率和持续时间,中断的持续时间以及总的治疗时间。
2.考虑到可能影响设备使用及其结局的特定前提条件,例如糖尿病,影响皮肤感觉,循环系统疾病的条件或与热/冷疗法结合使用时可能产生负面影响的某些药物。
3.使用设备时:应在设备包装纸和患者皮肤之间放置一个额外的屏障,以防止在整个使用设备期间包装纸接触皮肤。包装纸不应太紧。在整个治疗过程中,治疗部位应保持干燥。
4.如果患者面临任何不良反应(例如疼痛,肿胀,变色或灼伤),请暂停使用循环水热/冷治疗设备。
FDA认证对医疗保健专业人员的建议 :
除了针对患者的建议外,FDA认证安全通讯还包含针对在医疗保健和治疗过程中使用热/冷疗法医疗设备的医疗保健专业人员的建议。尽管没有以前的详细说明,但针对医疗保健提供者的建议描述了在使用水循环热/冷疗法医疗设备时要考虑的特定点。首先,FDA认证会参考医疗设备标签中指示的预防措施和警告,以描述应安全使用该设备的方式。医护人员应按照医疗设备制造商提供的使用说明使用设备。作为一项额外的安全措施,
FDA认证宣布将继续进行持续的监视活动,以确保允许在美国销售和使用的医疗设备的安全性,机构将适当地发布与水循环热/冷疗法医疗设备相关的安全问题的重要信息。此外,主管机关鼓励与医疗设备进行手术的所有有关方面报告所有不良事件和安全问题。特别是,面对副作用的设备的用户可以使用MedWatch自愿报告表或根据内部报告程序提交报告(如果由在适当机构工作的医护人员识别出副作用)。

一般报告程序
如今,医疗器械不良事件报告是根据FDA认证安全信息和不良事件报告计划建立的,可以通过两种方式进行:
1.通过在线报告门户提交报告,
2.通过提交填写好的FDA认证表格。
该机构指出,医疗保健专业人员应使用表格3500,而个人客户/患者应使用另一表格3500B。一旦开始,报告者将能够在报告过程开始之日起3天内完成报告。如果对应如何提供信息有任何疑问,记者可以提供联系方式并要求其他说明。
根据一般规则,要报告的信息范围包括:
1.使用医疗设备时出现不良事件或副作用,
2.与药品质量有关的问题,
3.与产品使用相关的问题(例如,由于标签问题而选择了错误的产品),
4.药品性能不当(治疗失败)。
根据适当的不良事件报告指南,报告者在提交报告时应提供以下信息:
1.有关问题本身的详细信息,
2.有关医疗设备的名称,
3.姓名。
据指出,可以包括其他细节,以简化和加快对不良事件报告的审查,但只有以上几点是强制性的。前提是所有必要的信息均已到位,填写报告表大约需要20分钟。记者提供的文字信息也可以附有图片(如有必要)。记者还可以要求当局不要向医疗设备制造商透露其名称。
填写的报告也可以由报告人打印以保存以备记录。提交不良事件报告时提供的所有信息均受安全套接字层(SSL)和安全防护(PGP)加密措施的保护。
总结以上提供的信息,关于水循环热/冷疗法医疗设备FDA认证的安全通讯根据特定型号描述了与使用此类设备相关的最常见风险,并概述了要考虑的建议由医疗保健提供者和患者。










